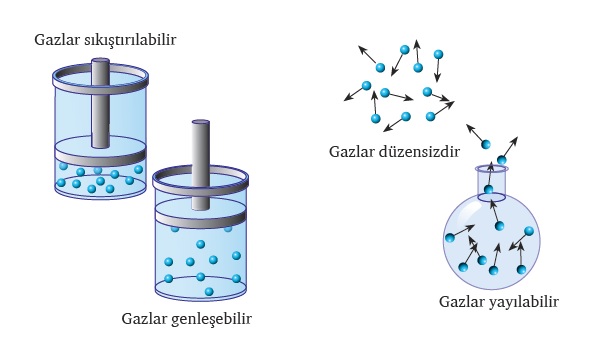
Gazları Tanımlayan Özellikler
Gazların farklı fiziksel davranışlar sergilemesi hacim, sıcaklık, basınç ve madde miktarı gibi değişkenlere bağlıdır. Gazlarda hacim birimi litre (L), basınç birimi atm ve mmHg, sıcaklık birimi Celcius (°C) ve Kelvin (K) ve miktar birimi de mol şeklindedir.
- Hacim (L)
- Sıcaklık (°C ve K)
- Basınç (atm ve mmHg)
- Madde miktarı (mol)
Basınç
Kapalı bir kap içerisindeki gazlar hem birbirlerine çarparak hem de kabın çeperine çarparak kuvvet uygularlar. Bu kuvvete gaz basıncı denir. Gaz basıncı da manometre ile ölçülür.
Basınç, birim yüzeye uygulanan kuvvettir. P ile gösterilir ve birimi de atmosfer (atm) ve mmHg’dir.
Basınç formülü;
Basınç (P) = Kuvvet (F) / Alan (S)
1 atm = 760 mmHg’dır.
Dünyamızı çevreleyen atmosferin yeryüzüne uyguladığı basınca atmosfer basıncı denir. Atmosfer bir gaz karışımıdır ve atmosfer basıncı barometre ile ölçülür.
Atmosfer basıncı yeryüzünün her noktasında aynı değildir. Atmosfer basıncı deniz seviyesinde 1’dir. Deniz seviyesinden yukarıya çıkıldıkça atmosfer basıncı düşer, deniz seviyesinden aşağıya inildikçe atmosfer basıncı artar. Örneğin atmosfer basıncı dağın zirvesine çıktıkça azalır ve denizin derinliklerine daldıkça artar.
Gaz basıncını etkileyen faktörler şunlardır;
- Birim hacimdeki gaz taneciği sayısı,
- Gaz moleküllerinin öteleme hareketi yani kinetik enerjisi,
- Gaz moleküllerinin hızı ve çarpma şiddeti,
- Gaz moleküllerinin saniyede çarpma sayısı.
Sıcaklık
Gazlarda sıcaklığı ölçmek için termometre kullanılır. Gazlarda sıcaklık ölçü birimi Kelvin (K) ve Celsius’dur (°C).
Mutlak Sıcaklık: Bir gazın Kelvin cinsinden sıcaklığına mutlak sıcaklık denir ve T ile gösterilir.
Normal Sıcaklık: Gazların Celsius (°C) cinsinden sıcaklığını gösterilmesidir ve t ile gösterilir.
- Gazların sıcaklığı arttıkça gaz taneciklerinin hızı ve ortalama kinetik enerjisi artar.
- Gazların sıcaklığı azaldıkça gaz taneciklerinin hızı ve ortalama kinetik enerjisi azalır.
- Aynı sıcaklıkta tüm gazların ortalama kinetik enerjisi aynıdır.
Kelvin (K) = Celcius (oC) + 273
T (K) = t (°C) + 273 şeklindedir.
Hacim
Gazların konuldukları kabın hacmine sahip olur. Hacim birimi litredir ve sembolü de V’dir.
Gazların hacminden bahsedebilmek için sıcaklık ve basınç olması gerekir. Çünkü gazlar sadece sıcaklık ve basınç altında bir hacme sahiptirler. Dolayısı ile gazların hacminin sıcaklık ve basınç ile değiştiğini söylemek gerekir. Bir gazın hacmini ölçmek istiyorsak, o gazın hangi sıcaklık ve basınç değerlerine sahip olduğunu da bilmemiz gerekir.
Oda Koşulları: Bir gazın 1 atm basınç ve 25 °C sıcaklık altında olması demektir.
Normal Koşullar: Bir gazın 1 atm basınç ve 0 °C sıcaklık altında olması demektir.
Avogadro Sayısı (NA): Normal koşullarda 1 mol gazda bulunan tanecik sayısına (6,02×1023) denir.
Örneğin bütün gazların 1’er molleri;
- Oda koşullarında 24,5 L hacim kaplar
- Normal koşullarda 22,4 L hacim kaplar.
Madde Miktarı
Bir madde içerisindeki tanecikleri tek tek saymak imkansızdır. Çünkü madde içerisinde sayılmayacak kadar atom veya molekül bulunur. Bu atom ve moleküller ise çok küçük taneciklidirler.
Kimyadaki ölçü birimlerinden birisi de moldür. Atom ve molekül gibi çok küçük ve sayısız taneciği ifade etmek için mol kullanılır.
Aynı sıcaklık ve basınca sahip bütün gazların 1’er molünde 6,02 x 10²³ tane molekül ya da atom bulunur.
1 mol = 6,02×1023 tane tanecik
1 Mol: Karbon-12 izotopunun 12 gramı içinde bulunan atom sayısına eşit, atom veya molekül içeren gazın madde miktarına 1 mol denilmiştir. Mol simgesi n harfidir ve 1 mol gazın mol kütlesi de MA şeklinde gösterilir.
Gazların madde miktarını hesaplarken, mol sayısı ve mol kütlesi işleme katılır. Eşit hacme sahip farklı gazların eşit sayıda taneciği bulunur.
Gazları Tanımlayan Özellikleri İle İlgili Sorular
Bu konuda öğrendiklerimizi sorularla pekiştirelim. Aşağıdaki sorulara cevap verebiliyorsanız, konuyu anlamışsınız demektir.
1. Gazları etkileyen faktörler nelerdir?
2. Gazları tanımlayan özelliklerden basınç nedir?
3. Gazları tanımlayan özelliklerden sıcaklık nedir?
4. Gazları tanımlayan özelliklerden hacim nedir?
5. Gazları tanımlayan özelliklerden madde miktarı nedir?
6. Gaz basıncı nedir?
7. Mutlak sıcaklık nedir?
8. Mol nedir?